|
第二节
肿瘤形成
肿瘤形成(oncogenesis)的过程包括始发突变、潜伏、促癌和演进。始发突变是指细胞在致癌物的作用下发生了基因突变,但是突变发生后如果没有适当的环境不会发展为肿瘤,此阶段称为潜伏期;促癌是指在促癌剂(刺激细胞增长的因子,如激素)作用下开始增殖的过程,促癌因子的作用是可逆的,如果去除,引起扩增的克隆就会消失;演进是指肿瘤在生长过程中越来越变得具有侵袭力的过程,是不可逆的。肿瘤形成往往涉及许多基因的突变,需要十到数十年的时间,因而恶性肿瘤通常属于老年性疾病。。
一、肿瘤形成的内因
恶性肿瘤的形成往往涉及多个基因的改变,与原癌基因、抑癌基因突变的逐渐积累有关。
原癌基因(oncogene)是细胞内与细胞增殖相关的基因,是维持机体正常生命活动所必须的,在进化上高等保守。当原癌基因的结构或调控区发生变异,基因产物增多或活性增强时,使细胞过度增殖,从而形成肿瘤。
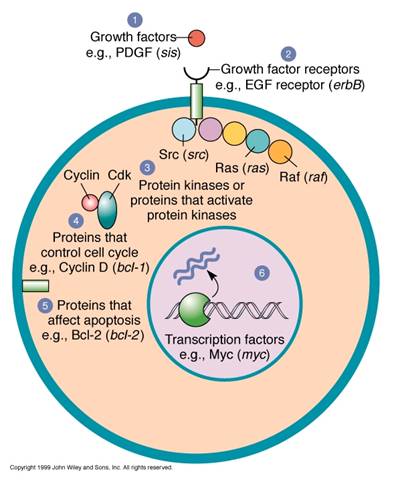
图16-3 原癌基因的产物 引自
原癌基因的产物主要包括(图16-3):①生长因子,如sis,②生长因子受体,如fms、erbB,③蛋白激酶及其它信号转导组分,如src、ras、raf,④细胞周期蛋白,如bcl-1,⑤细胞凋亡调控因子,如bcl-2,⑥转录因子,如myc、fos、jun。
表16-1 一些原癌基因的功能
|
原癌基因 |
功能 |
相关肿瘤 |
|
sis |
生长因子 |
Erwing网瘤 |
|
erb-B
|
受体酪氨酸激酶,EGF受体 |
星形细胞瘤、乳腺癌、卵巢癌、肺癌、胃癌、唾腺癌 |
|
fms
|
受体酪氨酸激酶,CSF-1 受体
|
髓性白血病 |
|
ras |
G-蛋白 |
肺癌、结肠癌、膀胱癌、直肠癌 |
|
src |
非受体酪氨酸激酶 |
鲁斯氏肉瘤 |
|
Abl-1 |
非受体酪氨酸激酶 |
慢性髓性白血病 |
|
raf |
MAPKKK,丝氨酸/苏氨酸激酶 |
腮腺肿瘤 |
|
vav |
信号转导连接蛋白 |
白血病 |
|
myc |
转录因子 |
Burkitt
淋巴瘤、肺癌、早幼粒白血病 |
|
myb |
转录因子 |
结肠癌 |
|
fos |
转录因子 |
骨肉瘤 |
|
jun |
转录因子 |
|
|
erb-A |
转录因子 |
急性非淋巴细胞白血病 |
|
bcl-1 |
cyclinD1 |
B细胞淋巴瘤 |
早在1911年Rous发现鸡肉瘤无细胞滤液能引起鸡产生新的肉瘤,几十年后,他证实了病原体为罗氏病毒(Rous’s sarcoma virus, RSV),为此获得1966年的诺贝尔奖。1970年Temin 和Batimore证实RSV是一种反转录病毒,获1975年诺贝尔奖。
1970s H. Varmus和J. M. Bishop研究小组发现RSV中的致瘤基因是src基因,但是用src的cDNA(complementary DNA)和其他基因组DNA杂交,发现src的同源物普遍存在于动物细胞(如鸡、鸭、果蝇)。原来src编码一种胞质酪氨酸激酶,参与细胞增殖相关的信号转导,是细胞的正常组分。由于RSV、ASV等反转录病毒的基因组是整合在宿主基因组上复制的,会将宿主的某些基因复制到了自身的基因组中,因此被这样的病毒感染的细胞,src基因拷贝就增多了,引起细胞过度增殖。为了区别起见将存在于正常细胞中的癌基因序列称为c-onc,而把存在于病毒中的称为v-onc。从结构上看c-onc是间断的,存在内含子,这是真核基因的特点。而v-onc是连续的,基因跨度较小。
抑癌基因也称为抗癌基因。早在1960s,有人将癌细胞与同种正常成纤维细胞融合,所获杂种细胞的后代只要保留某些正常亲本染色体时就可表现为正常表型,但是随着染色体的丢失又可重新出现恶变细胞。这一现象表明,正常染色体内可能存在某些抑制肿瘤发生的基因,它们的丢失、突变或失去功能,使激活的癌基因发挥作用而致癌。
抑癌基因的产物是抑制细胞增殖,促进细胞分化,和抑制细胞迁移,因此起负调控作用,通常认为抑癌基因的突变是隐性的。
抑癌基因的产物主要包括(表16-2):①转录调节因子,如Rb、p53;②负调控转录因子,如WT;③周期蛋白依赖性激酶抑制因子(CKI),如p15、p16、p21;④信号通路的抑制因子,如ras GTP酶活化蛋白(NF-1),磷脂酶(PTEN);⑥DNA修复因子,如BRCA1、BRCA2。⑥与发育和干细胞增殖相关的信号途径组分,如:APC、Axin等。
抑癌基因失活的途径:①等位基因隐性作用,失活的抑癌基因之等位基因在细胞中起隐性作用,即一个拷贝失活,另一个拷贝仍以野生型存在,细胞呈正常表型。只有当另一个拷贝失活后才导致肿瘤发生,如Rb基因。②抑癌基因的显性负作用(dominant negative):抑癌基因突变的拷贝在另一野生型拷贝存在并表达的情况下,仍可使细胞出现恶性表型和癌变,并使野生型拷贝功能失活。这种作用称为显性负作用或反显性作用。如近年来证实突变型p53和APC蛋白分别能与野生型蛋白结合而使其失活,进而转化细胞。③单倍体不足假说(Haplo-insufficiency):某些抗癌基因的表达水平十分重要,如果一个拷贝失活,另一个拷贝就可能不足以维持正常的细胞功能,从而导致肿瘤发生。如DCC基因一个拷贝缺失就可能使细胞粘膜附功能明显降低,进而丧失细胞接触抑制,使细胞克隆扩展或呈恶性表型。
表16-2 一些抑癌基因的功能
| 抑癌基因 |
功能 |
相关肿瘤 |
|
Rb |
转录调节因子 |
RB、成骨肉瘤、胃癌、SCLC、乳癌、结肠癌 |
|
p53 |
转录调节因子 |
星状细胞瘤、胶质母细胞瘤、结肠癌、乳癌、成骨肉瘤、SCLC、胃癌、磷状细胞肺癌 |
|
WT |
负调控转录因子 |
WT、横纹肌肉瘤、肺癌、膀胱癌、乳癌、肝母细胞瘤 |
|
NF-1 |
GAP,ras GTP酶激活因子 |
神经纤维瘤、嗜铬细胞瘤、雪旺氏细胞瘤、神经纤维瘤 |
|
DCC |
细胞粘附分子 |
直肠癌、胃癌 |
|
p21 |
CDK抑制因子 |
前列腺癌 |
|
p15 |
CDK4、CDK6抑制因子 |
成胶质细胞瘤 |
|
BRCA1 |
DNA修复因子,与RAD51作用 |
乳腺癌、卵巢癌 |
|
BRCA2 |
DNA修复因子,与RAD51作用 |
乳腺癌、胰腺癌 |
|
PTEN |
磷酯酶 |
成胶质细胞瘤 |
|
APC |
WNT信号转导组分 |
结肠腺瘤性息肉,结/直肠癌 |
Rb(人类视网膜细胞瘤)基因是第一个被克隆的抑癌基因。Rb的突变导致视网膜瘤。散发性Rb发生较晚,一般只危及一眼,遗传性Rb往往危及双眼,3岁左右发病形成多个肿瘤(图16-4)。在G1期Rb与E2F结合,抑制E2F的活性,在G1/S期Rb被CDK2磷酸化失活而释放出转录因子E2F,促进蛋白质的合成(图16-5)。
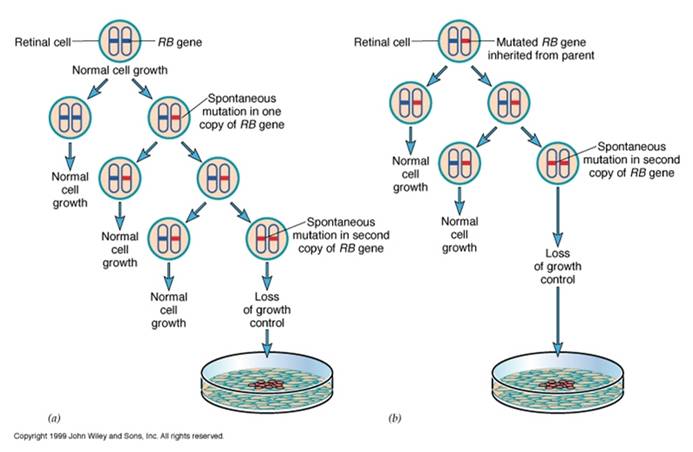
图16-4
散发性和遗传性Rb功能丧失的机理
APC基因最初是在结肠腺瘤样息肉(adenomatous
polyposis coli)病人中发现的,并以此命名。APC基因定位于染色体5q21-22,属于Wnt信号途径的负调控因子,APC蛋白可与β-catenin连接,促进β-catenin降解,而β-catenin在细胞内积累后,可进入细胞核,与T细胞因子TCF结合,促进相关基因的表达。
DCC基因亦称结直肠癌缺失基因(deleted in colorectal carcinoma),氨基酸顺序与神经细胞粘附分子(N-CAM)及其它相关的细胞表面糖蛋白十分相似。该基因失活,可导致细胞的生物学行为,如细胞粘附、接触性抑制及运动发生重要改变,使细胞朝恶性化方向演变,并容易发生转移,DCC基因在胃癌中的缺失率为40%~60%左右。
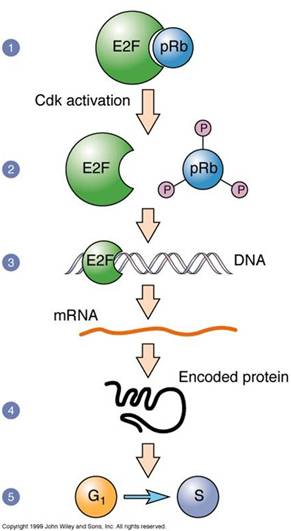
图16-5 Rb基因的作用
恶性肿瘤的发生归根到底是因为原癌基因的激活和抑癌基因的功能丧失,往往涉及多个基因的改变。原癌基因的激活方式多种多样,但概括起来无非是基因本身或其调控区发生了变异,导致基因的过表达,或产物蛋白活性增强,使细胞过度增殖,形成肿瘤(图16-6)。如在肝癌中cyclinA过渡表达,在乳腺癌中常有cyclinA、B、D1、E等过渡表达。
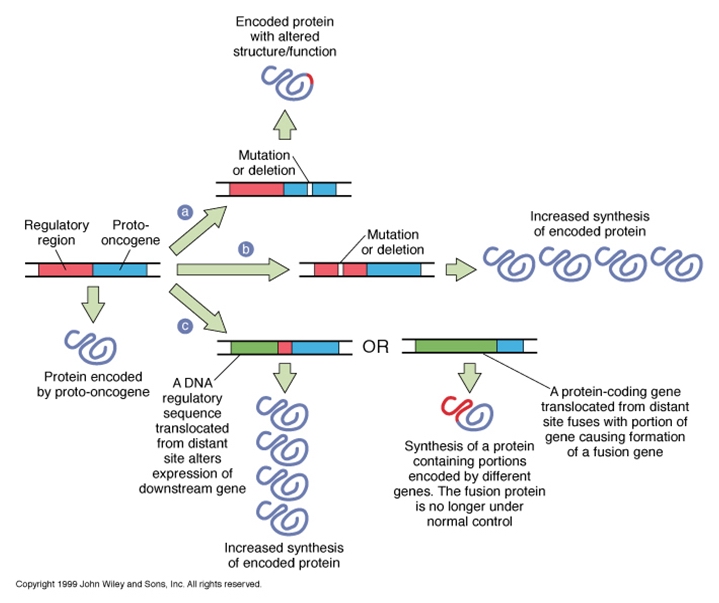
图16-6 原癌基因激活的可能途径
1.点突变
ras基因家族,均以点突变为主,如膀胱癌细胞中克隆出来的c-Ha-ras基因与正常细胞的相比仅有一个核苷酸的差异。
2.DNA重排
原癌基因在正常情况下表达水平较低,但当发生染色体的易位或倒位时,处于活跃转录基因强启动子的下游,而产生过度表达。如Burkitt淋巴瘤细胞的染色体易位,使c-myc与IG重链基因的调控区为邻,由于免疫球蛋白重链基因表达十分活跃,其启动子为强启动子,且在CH-VH之间还有增强子区,致使c-myc过表达。再如在良性甲状旁腺肿瘤患者的染色体中,cyclinD1基因倒位处于甲状旁腺素基因启动子下游而过渡表达,使细胞出现异常增殖。
染色体易位的主要原因是人类染色体存在着脆性位点,而染色体重排的断裂热点多位于脆性位点。恶性肿瘤的染色体重排是获得性的体细胞变化,而不是发生在生殖细胞内的变化。
3.插入激活
某些不含v-onc的弱转化逆转录病毒,其前病毒DNA插入宿主DNA中,引起插入突变,如逆转录病毒MoSV感染鼠类成纤维细胞后,病毒两端各有一个相同的冗长末端重复序列(LTR),它们不编码蛋白质,而含有启动子、增强子等调控成分,病毒基因组的LTR整合到细胞癌基因c-mos邻近处,使c-mos处于LTR的强启动子和增强子作用之下而被激活,导致成纤维细胞转化为肉瘤细胞,再如鸟类白血病病毒ALV不含v-onc,但插入c-myc的上游,导致基因过度表达。
4.基因扩增
在某些造血系统恶性肿瘤中,癌基因扩增是一个极常见的特征,如前髓细胞性白血病细胞系和这类病人的白血病细胞中,c-myc扩增8~32倍。癌基因扩增的染色体结构有:①双微体(double minute chromosomes,DMs),无着丝粒,成对分布于细胞中的微小染色体(图16-7);②均染区(homogenously stained region,HSR),是染色局部扩增形成的(图16-8);③姊妹染色单体非均等交换(unequal sister chromatid
exchange,USCE),G2期由于姊妹染色单体之间发生了非均等交换,结果一个子细胞中该染色体较长,具有同源重复(基因扩增),另一个细胞中对应的染色体较短(基因删除)。其中DMS和HSR是最常见的类型,在具有DMS或HSR的直肠癌患者中c-myc mRNA含量是正常人的30倍。
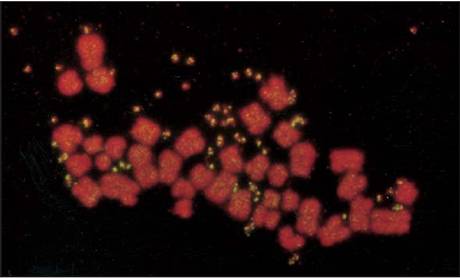
图16-7
Myc基因扩增形成双微核(黄色)的核型 引自Molecular
Biology of the Cell. 4th ed. 2002
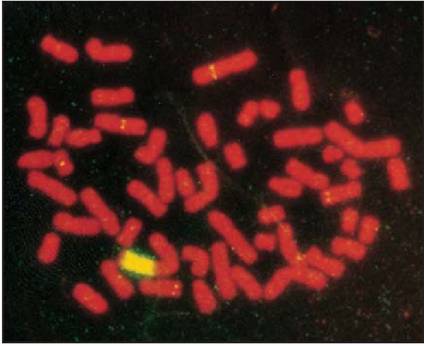
图16-8 Myc基因扩增形成均染区(黄色)的核型 引自Molecular
Biology of the Cell. 4th ed. 2002
5、原癌基因的低甲基化
致癌物质的作用下,使原癌基因的甲基化程度降低而导致癌症,这是因为致癌物质降低甲基化酶的活性。
人类肿瘤约80%是由于与外界致癌物质接触而引起的,根据致癌物的性质可将其分为化学、生物和物理致癌物三大类。根据它们在致癌过程中的作用,可分为启动剂、促进剂、完全致癌物。
启动剂是指某些化学、物理或生物因子,它们可以直接改变细胞遗传物质DNA的成分或结构,一般一次接触即可完成,其作用似无明确的阈剂量,启动剂引起的细胞改变一般是不可逆的。
促进剂本身不能诱发肿瘤,只有在启动剂作用后再以促进剂反复作用,方可促使肿瘤发生(图16-9)。例如用启动剂二甲基苯并蒽(dimethytenzanthracene,DMBA)涂抹动物皮肤并不致癌,但是几周后再涂抹巴豆油,则引起皮肤癌,巴豆油中的有效成分是佛波醇酯,能模仿二酰基甘油(DAG)信号,激活蛋白激酶C。促癌物的种类很多,如某些激素、药物等。有的促癌物只对诱发某种肿瘤起促进作用,而对另一种肿瘤的发生不起作用,例如糖精可促进膀胱癌的发生,但对诱发肝癌不起促进作用;苯巴比妥促进肝癌的发生,但不促进膀胱癌的发生。
有些致癌物的作用很强,兼具启动和促进作用,单独作用即可致癌。称为完全致癌物。如多环芳香烃、芳香胺、亚硝胺、致癌病毒等。
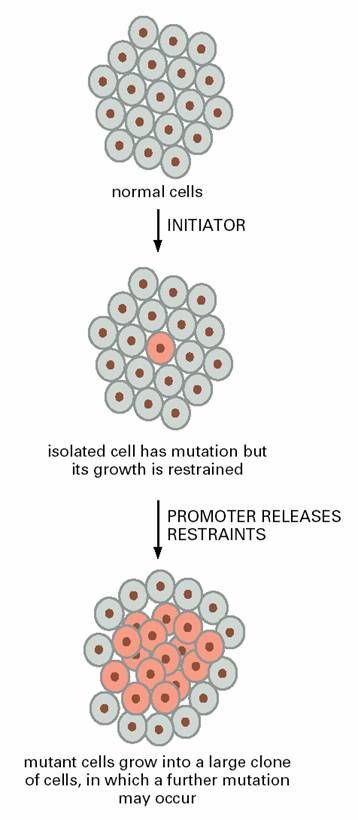
图16-9
启动与促癌 引自Molecular
Biology of the Cell. 4th ed. 2002
按化学结构可分为:①亚硝胺类,这是一类致癌性较强,能引起动物多种癌症的化学致癌物质。在变质的蔬菜及食品中含量较高,能引起消化系统、肾脏等多种器官的肿瘤;②多环芳香烃类,这类致癌物以苯并芘为代表,将它涂抹在动物皮肤上,可引起皮肤癌,皮下注射则可诱发肉瘤。这类物质广泛存在于沥青、汽车废气、煤烟、香烟及熏制食品中;③芳香胺类,如乙萘胺、联苯胺、4-氨基联苯等,可诱发泌尿系统的癌症;④烷化剂类,如芥子气、环磷酰胺等,可引起白血病、肺癌、乳腺癌等;⑤氨基偶氮类,如用二甲基氨基偶氮苯(即奶油黄,可将人工奶油染成黄色的染料)掺入饲料中长期喂养大白鼠,可引起肝癌;⑥碱基类似物,如5-溴尿嘧啶、5-氟尿嘧啶、2-氨基腺嘌呤等,由于其结构与正常的碱基相似,进入细胞能替代正常的碱基参入到DNA链中而干扰DNA复制合成;⑦氯乙烯,目前应用最广的一种塑料聚氯乙烯,是由氯乙烯单体聚合而成。大鼠长期吸入氯乙烯气体后,可诱发肺、皮肤及骨等处的肿瘤。通过塑料工厂工人流行病学调查已证实氯乙烯能引起肝血管肉瘤,潜伏期一般在15年以上;⑧某些金属,如铬、镍、砷等也可致癌。
化学致癌物引起人体肿瘤的作用机制很复杂。少数致癌物质进入人体后可以直接诱发肿瘤,这种物质称为直接致癌物。大多数化学致癌物进入人体后,需要经过体内代谢活化或生物转化,成为具有致癌活性的最终致癌物,才能引起肿瘤发生,这种物质称为间接致癌物。在体内参与此类化合物代谢的主要为P450酶系。
最终致癌物通常为亲电分子,可与DNA、RNA、蛋白质等生物大分子中的亲核基团发生作用,引起碱基颠换、缺失,DNA交联、断裂,染色体畸变等。化学致癌物还可抑制甲基化酶,引起细胞中胞嘧啶的甲基化水平降低,还有可能激活某些癌基因,使细胞癌变。
直接或间接导致DNA发生突变的致癌物称为基因毒性致癌物(genotoxic carcinogen),上述提到的化学致癌物均属于此类。但是乳腺癌、前列腺癌和子宫膜癌的致癌物是有激素活性的甾体类化合物,它们并不损伤基因,但能促进细胞分裂,称为非基因毒性致癌物(non-genotoxic carcinogen),如雌二醇可引起卵巢癌和乳腺癌。由此可见并不是所有的致癌物都是诱变剂,当然也并非所有的诱变剂都是致癌的,譬如某也碱基类似物能引起微生物变异,但不引起实验动物的癌症。
生物性致癌因素包括病毒(图16-10)、细菌、霉菌等。其中以病毒与人体肿瘤的关系最为重要,研究也最深入。
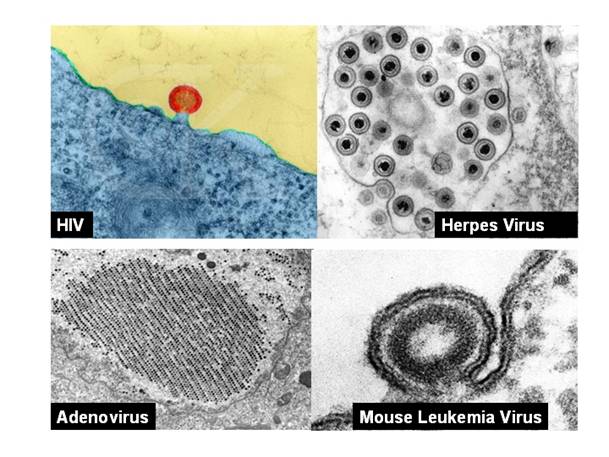
图16-10
一些肿瘤相关的病毒
1.肿瘤病毒:
与人类肿瘤发生关系密切的有四类病毒:①逆转录病毒(如T细胞淋巴瘤病毒,HTLV-I)、②乙型肝炎病毒(HBV)、③乳头状瘤病毒(HPV)和④Epstein-Bars病毒(EBV),后三类都是DNA病毒。
逆转录病毒:引起人类T淋巴细胞白血病的人T淋巴细胞白血病病毒(HTLV)、成人 T细胞白血病病毒(ATLV)和爱滋病病毒(HIV)等病毒都属于逆转录病毒。逆转录病毒感染机体后,病毒的遗传信息整合到宿主细胞的染色体中,成为细胞的组成部分,一般情况下受到正常细胞的调节控制,病毒处于静止状态,但受到化学致癌物、射线辐射等因素的作用后,可能被激活病毒表达而在体内诱发肿瘤。
乙型肝炎病毒:人肝癌细胞DNA中发现有HBV病毒的碱基序列。体外培养的人肝癌细胞中,见到HBV病毒DNA整合到细胞DNA中。HBV整合到细胞 DNA中,能使细胞 DNA发生缺失、插入、转位、突变或易位等改变。
乳头状瘤病毒:人乳头瘤状病毒(human papilloma virus,HPV)有 50余种亚型,与生殖道肿瘤的发生有密切关系,并与口腔、咽、喉、气管等处的乳头状瘤和皮肤疣等良性病变有关。在宫颈癌细胞中病毒DNA序列已经整合到宿主细胞的基因组中,宫颈癌的发生与原癌基因c-ras和c-myc的变异有关。
EB病毒:EB病毒(Epstein-Barr virus,EBV)是一种疱疹病毒,与儿童的 Burkitt淋巴瘤和成人的鼻咽癌发生有关。
2.霉菌与肿瘤发生
目前已知有数十种霉菌毒素对动物有致癌性。但除黄曲霉毒素(aflatoxin)外,对其它的研究都较少。黄曲霉菌广泛存在于污染的食品中,尤以霉变的花生、玉米及谷类含量最多。黄曲霉毒素有许多种,是一类杂环化合物,其中黄曲霉毒素B1是已知最强的化学致癌物之一,可引起人和啮齿类、鱼类、鸟类等多种动物的肝癌。
1.电离辐射
电离辐射可以引起人体各部位发生肿瘤,但据估计在所有肿瘤的总病例数中只占2%~3%左右。居里夫人的去世,日本原子弹爆炸后引起白血病的发病率增高,都是著名的例子。
辐射可引起染色体、DNA的突变,或激活潜伏的致癌病毒。放射线引起的肿瘤有:白血病、乳腺癌、甲状腺肿瘤、肺癌、骨肿瘤、皮肤癌、多发性骨髓瘤、淋巴瘤等。
2.紫外线
紫外线照射可引起细胞DNA断裂、交联和染色体畸变,紫外线还可抑制皮肤的免疫功能,使突变细胞容易逃脱机体的免疫监视,这些都有利于皮肤癌和基底细胞癌的发生。近年来由于环境恶化,大气层的臭氧减少,出现地球臭氧空洞,地表紫外线的辐照强度将急剧增高,其诱发人体皮肤癌的潜在危险性将大为增加。据估计,大气臭氧减少1%,皮肤癌就要增加2-6%。
三、肿瘤的起源与演进
对肿瘤的起源有两种见解,其一是认为来源于去分化的体细胞,其二是认为来源于干细胞。虽然在某些低等动物中已分化的细胞可以去分化,但是在哺乳动物中通常已分化的细胞不再具备自我更新(self-renewal)能力,即使发生突变也只是功能异常而不致于转化,而干细胞是一直存在的,并不断更新,突变更容易在干细胞中累积,所以现在普遍倾向于认为肿瘤来源于恶性干细胞。有些组织,如肝、肾虽然不具有干细胞,但是其细胞在特殊情况下也具有分裂能力,因而也是致癌物的靶细胞。
干细胞是体内具有定向分化能力和分裂能力的细胞,如骨髓细胞可以分化出各种血细胞。肿瘤细胞和干细胞有很多相似之处,如:均有自我更新和无限增殖的能力;较高的端粒酶活性;相同的调节自我更新的信号转导途径,如Wnt、Hedgehog、Notch、NF-κB等信号途径(图16-11)。
Hedgehog信号通道参与早期神经系统发育和毛囊形成的调控。Hedgehog途径中的抑制物突变后,信号系统活性增高,可诱导中枢神经系统肿瘤的产生,如Patched基因突变,可引起Gorlin’s综合征和小鼠的小脑肿瘤。Notch信号通路调控造血干细胞的自我更新,通过抑制造血干细胞的特定分化阶段,控制造血干细胞向粒系或淋巴系分化,Notch信号通路的过度表达可诱导恶性淋巴瘤的产生。在黑色素瘤和一些肠道肿瘤中存在异常Wnt信号,尤其是Wnt途径的组成成分,如β-catenine、APC、Axin等发生基因突变。
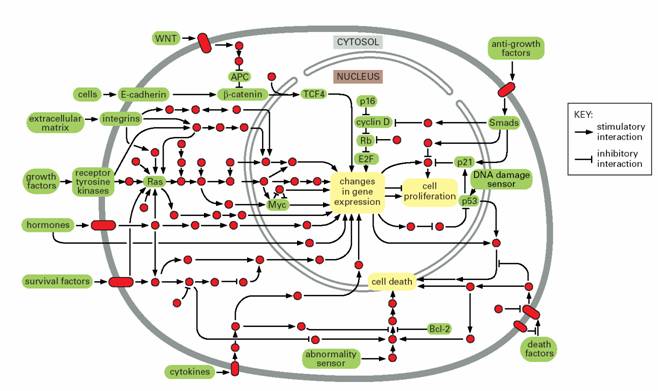
图16-11
引起肿瘤的信号途径 引自Molecular Biology of the
Cell. 4th ed. 2002
多数肿瘤来源于单克隆细胞,如在女性中,胚胎发育时期,细胞中的一个X染色体随机失活,某些X染色体连锁的酶(如葡糖-6-磷酸脱氢酶)在组织中具有异质性,即:不同细胞中表达不同的同工酶,而在肿瘤细胞中却是相同的,从这一点上来看一个肿瘤中的细胞具有相同的起源(图16-12)。
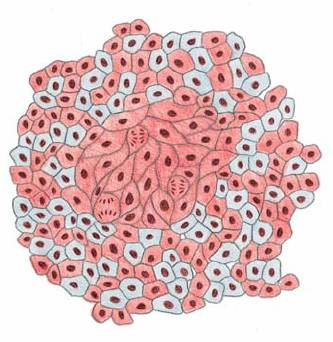
图16-12
女性巴氏体证明肿瘤起源于单克隆 引自Molecular Biology of the Cell. 4th ed. 2002
前面提到肿瘤的形成涉及多个基因的突变,因而是一个渐进的复杂过程。多次突变形成肿瘤细胞的异质性,其中少量的细胞具有很强的增值能力,被称为肿瘤干细胞(tumor stem cell)。早在70年代Park等研究发现从小鼠腹水中分离得到的骨髓瘤细胞移植体内,只有1%到4%的骨髓瘤细胞能在脾脏形成克隆,这些骨髓瘤细胞与通常造血细胞一样,只有少量的细胞能形成克隆,这些能形成克隆的骨髓瘤细胞很可能就是骨髓瘤干细胞。
当前肿瘤治疗的目的是尽可能杀死所有肿瘤细胞,认为每个肿瘤细胞都有无限增殖能力,如果肿瘤体积缩小认为治疗方案有效。但实际上大部分肿瘤经过一段时间缓解期后又复发。根据干细胞理论,这种传统的治疗方法并没有将肿瘤干细胞完全杀死,仍具有无限增殖能力。越来越多的学者提出肿瘤治疗应该针对肿瘤干细胞,即使肿瘤体积没有缩小,但由于其他细胞增殖能力有限,肿瘤将逐渐退化萎缩,也许人类能够真正治愈肿瘤。
|